De acuerdo con el estudio realizado por Li Guo y cols. En la revista Clinical Infectious Diseases, Publicado en línea el 21 de marzo de 2020 del Institute of Pathogen Biology, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing, China, Donde el objetivo fue describir la cinética temporal de varios anticuerpos producidos contra el nuevo coronavirus 2019 (SARS-CoV-2) y evaluar el potencial de las pruebas de anticuerpos para diagnosticar COVID-19.

Mediante la reacción en cadena de la polimerasa (PCR) en comparación de la aparición de anticuerpos IgM, IgA e IgG contra el SARS-CoV-2, mencionando que la PCR es un método de detección que depende en gran medida de la presencia del genoma viral en cantidades suficientes en el sitio de recolección de muestras para que pueda amplificarse otro factor sería perder la ventana de tiempo de la replicación viral y puede proporcionar resultados falsos negativos. Del mismo modo, una recolección de muestra incorrecta puede limitar la utilidad del análisis cuantitativo basado en PCR (qPCR). Esto es importante ya que un diagnóstico falso negativo puede tener graves consecuencias, especialmente en esta etapa de la pandemia, al permitir que los pacientes infectados propaguen la infección y obstaculicen los esfuerzos para contener la propagación del virus. En tales condiciones, los métodos de detección adicionales que pueden detectar la presencia de infección a pesar de los títulos virales más bajos pueden ser muy beneficiosos para garantizar el diagnóstico oportuno de todos los pacientes infectados. La detección de la producción de anticuerpos, especialmente la inmunoglobulina IgM, que se producen rápidamente después de la infección, puede ser una herramienta que se puede combinar con PCR para mejorar la sensibilidad y la precisión de la detección.
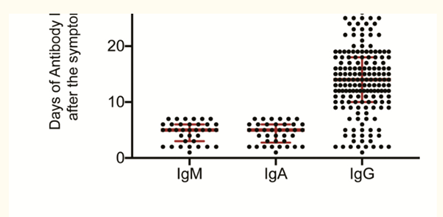
De un total de 208 muestras de sangre de 2 cohortes se encontró que la aparición de anticuerpos IgM, IgA e IgG contra el SARS-CoV-2 fue positiva tan pronto como el día 1 después del inicio de los síntomas (Fig.1). Como la IgM es un marcador de infección aguda, se examinaron específicamente la positividad de la IgM anti-SARS-CoV-2 en las 41 muestras de plasma que se recolectaron dentro de los 7 días de haber iniciado los síntomas, lo que puede representar muestras de fase aguda. En base a estas muestras de fase aguda, los anticuerpos IgM e IgA fueron detectables en el día 5 (mediana; rango Inter cuartil [RIQ], 3-6 días), respectivamente. Los anticuerpos IgG anti-SARS-CoV-2 fueron positivos en 162 (77,9%) muestras de plasma. La mediana del tiempo de aparición de IgG fue en el día 14 (RIC, 10-18 días) de haber iniciado los síntomas Los tiempos de detección de IgM, IgA e IgG contra SARS-CoV-2 oscilaron entre el día 1 y el 39 PSO en nuestro estudio (datos no mostrados).
En general, la tasa de detección por qPCR fue mayor que el ELISA de IgM antes de 5,5 días de haber iniciado los síntomas, mientras que la eficiencia de detección por ELISA de IgM fue mayor que la del método de PCR después de 5,5 días de inicio de los síntomas. En general, la tasa de detección positiva fue solo del 51,9% en una sola prueba de PCR, pero aumentó significativamente (98,6%) cuando se aplicó un ensayo ELISA IgM a pacientes con PCR negativa (Figura 2)
Ellos proponen realizar pruebas de anticuerpos cuando una prueba de qPCR es negativa a pesar de otras indicaciones de COVID-19, incluidos los síntomas y la epidemiología. Los datos muestran que la prueba de IgM suplementaria puede proporcionar una mejor sensibilidad que un método basado en qPCR solo. Aunque un qPCR es más sensible puede mejorar la eficacia de detección, la eficacia aún puede estar limitada debido a varias razones biológicas como se discutió anteriormente. Sin embargo, los ensayos de qPCR más sensibles pueden mejorar aún más el método de detección cuando se combinan con ELISA de IgM.

Como conclusión personal:
1.- El PCR dentro de los primeros días (1 a 5 días) de haber iniciado los síntomas es confiable, siempre y cuando se ha realizado una buena toma de muestra y no se haya confundido el período de ventana.
2.- Las pruebas rápidas por ELISA que determinan anticuerpos IgM, IgA, IgG, detectan y son positivas de los primeros días de haber iniciado los síntomas.
3.- Siendo la IgM y la IgA determinante como indicado de la fase aguda como mediana en el día 5.
4.- Es la IgG determinantes como indicador de la fase de memoria, marcando la aparición desde los primeros días de haber iniciador, pero su mediana es el día 14 más confiable.
5.- Ante un falso negativo la conducta adecuada sería la determinación de los anticuerpos IgM, IgA & IgG.
6.- La combinación de qPCR más Elisa IgM, aumenta la sensibilidad y especificidad en el diagnóstico.
Elaborado por:

Director General IREGA
